|
克唑替尼 赛可瑞 Crizotinib
收藏
药品名称: 【通用名称】 克唑替尼胶囊 [药典] 【商品名称】 赛可瑞 【英文名称】 Crizotinib Capsules 【汉语拼音】 Kezuotini Jiaonang
成份: 本品主要成份为克唑替尼 其化学名称为: (R)-3-[1-(2,6-二氯-3-氟-苯)-乙氧基]-5-(1-哌啶-4-烃基-1 氢-吡唑-4-烃基)-嘧啶-2-茚满 化学结构式:
分子式: C21H22Cl2FN5O 分子量: 450.34 道尔顿 辅料名称:二氧化硅、微晶纤维素、无水磷酸氢钙、羧甲基淀粉钠、硬脂酸镁。
性状: 本品为胶囊剂,内容物为白色至淡黄色粉末。
适应症: 克唑替尼胶囊可用于经 CFDA 批准的检测方法确定的间变性淋巴瘤激酶(ALK)阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者的治疗。
规格: (1) 250 mg;(2) 200 mg
用法用量: 患者选择 本品必须在有使用经验的医疗机构中并在特定的专业技术人员指导下使用。服用本品前,必须获得经充分验证的检测方法证实的ALK阳性评估结果。 推荐剂量 克唑替尼胶囊的推荐剂量为 250mg 口服,每日两次,直至疾病进展或患者无法耐受。对于无需透析的严重肾损害(肌酐清除率<30ml/分钟)患者,克唑替尼胶囊的推荐剂量为 250 mg 口服,每日一次。胶囊应整粒吞服。克唑替尼胶囊与食物同服或不同服均可。若漏服一剂克唑替尼胶囊,则补服漏服剂量的药物,除非距下次服药时间短于 6 小时。如果在服药后呕吐,则在正常时间服用下一剂药物。 剂量调整 如果患者出现美国国立癌症研究所(NCI)不良事件通用术语标准( CTCAE, 第 4.0 版)规定的严重程度为 3 级或 4 级的不良事件,需一次或多次减少剂量,按以下方法减少剂量: ·第一次减少剂量:口服,200 mg,每日两次 ·第二次减少剂量:口服,250 mg,每日一次 ·如果每日一次口服 250 mg 克唑替尼胶囊仍无法耐受,则永久停服 剂量减少指南参见表 1 和表 2。 表 1. 克唑替尼胶囊剂量调整——血液学毒性*
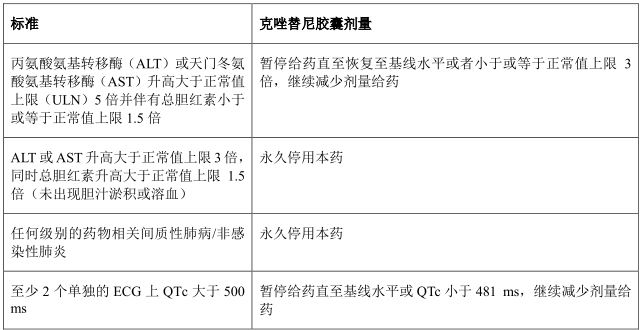
*淋巴细胞减少除外(除非伴随临床事件,例如,机会性感染)。 表 2. 克唑替尼胶囊剂量调整——非血液学毒性
应在每月和出现临床症状时监测包括白细胞分类计数的全血细胞计数,如果出现 3 或 4 级异常或发热或感染时,应增加监测频度。 肝损害患者 目前尚未对肝损害的患者使用克唑替尼的情况进行研究。由于克唑替尼主要在肝脏代谢,肝损害很可能升高克唑替尼的血浆浓度。因此,肝损害的患者使用克唑替尼胶囊进行治疗时应谨慎 。(见【药代动力学】) 肾损害患者 根据群体药代动力学分析, 对轻度 (肌酐清除率[CLcr]为 60 至 89 ml/分钟) 和中度 ([CLcr]为 30 至 59ml/分钟)肾损害的患者不需要进行起始剂量调整。在无需透析的严重肾损伤([CLcr]小于 30 ml/分钟)患者中,克唑替尼的暴露量增加,推荐克唑替尼起始剂量为 250 mg,口服,每日一次。 (见【药代动力学】项下“特殊人群”)
不良反应: 以下不良反应在说明书的其他部分有更加详细的论述: ·肝毒性 [见注意事项] 。 ·间质性肺病/非感染性肺炎 [见注意事项] ·QT 间期延长 [见注意事项] ·心动过缓 [见注意事项] 特定药物不良反应描述 视觉异常 在临床试验中(n=1225),691 例(56%)患者出现了视觉异常,最常见的有视觉损害、闪光幻觉、视物模糊或玻璃体飞蚊症。大多数(99%)患者都出现了 1 级或 2 级视觉不良反应。在临床研究中,1 例患者出现了 3 级治疗相关视觉异常。 此外,现行欧盟说明书**还报告了以下不良反应: 在研究 A8081007、 研究 A8081001 和研究 A8081005 中, 分别有 103 例(60%)、 99 例(66%)和 513 例(55%)患者在治疗期间出现全因果关系视觉异常,最常见的有视觉损害、闪光幻觉、视物模糊和玻璃体飞蚊症。研究 A8081007、A8081001 和 A8081005 分别报告该事件为轻度(96%)、中度(3%)和重度(< 1%),中位发生时间分别为 5 天、15 天和 7 天。研究 A8081007、A8081001 和研究 A8081005 分别有 0 例、1例和 4 例患者出现暂时中断治疗的情况。研究 A8081007 和研究 A8081005 各有 1 例患者因视觉异常减少剂量。研究 A8081007、A8081001 和 A8081005 均无患者因视觉异常需要永久停止克唑替尼治疗。如果视觉异常持续出现或加剧,应考虑进行眼科检查( 见 【注意事项】 ) 。 根据视觉症状评估问卷(Visual Symptom Assessment Questionnaire,VSAQ-ALK),研究 A8081007 中接受克唑替尼胶囊治疗的患者报告的视觉障碍发生率高于化疗组患者。视觉异常一般在用药的第一周内开始出现。研究 A8081007 中的大多数克唑替尼胶囊组患者(>50%)报告了视觉障碍;根据在患者问卷中获得的结果,这些视觉障碍的发生率为每周 4-7 天,最长持续 1 分钟,对日常生活有轻微影响或没有影响(评分为 0-3 分,最高分为 10 分)。 神经病变 在 1225 例患者中,有 235 例(19%)出现了神经病变,最常见的实际上为感觉神经病变。大多数事件(95%)的严重程度为 1 级或 2 级。 现行欧盟说明书还报告,味觉障碍也是这些研究报告的很常见的不良事件,严重程度主要为 1 级。 肾囊肿 在研究 A8081007 中,克唑替尼胶囊治疗组和化疗组患者中分别有 7 例(4%)和 1 例(1%)出现肾囊肿。接受克唑替尼胶囊治疗的患者出现的大部分肾囊肿为复杂性肾囊肿。观察到局部囊性侵及肾脏, 在某些病例中影像特征表明脓肿形成。但是,在临床试验中微生物检测均未确认肾脓肿。 此外,现行欧盟说明书还报告对于出现肾囊肿的患者,应考虑通过影像学检查和尿液分析进行定期监测。 肝毒性 目前已发生药物引起的致命性肝毒性,见于临床研究中少于 1%的接受克唑替尼胶囊治疗的患者。临床研究中少于 1%的患者观察到ALT 升高> 3倍ULN 同时伴有总胆红素> 2倍 ULN而碱性磷酸酶未升高。 在研究 A8081007 中,克唑替尼治疗组中有 17%的患者观察到 3 级或 4 级 ALT 升高,而化疗组中这一比例为 4%。 在研究 A8081001 和研究 A8081005 中, 分别有 7%和 8%的患者出现 3 级或 4 级 ALT 升高。 转氨酶 (ALT、 AST) 升高通常发生在治疗的前2个月。 在研究A8081001、 研究A8081005和研究A8081007中, 1 级或 2 级转氨酶升高的中位发生时间为 22 至 26 天。 3 级或 4 级转氨酶升高的中位发生时间为 30至 43 天。3 级和 4 级升高通常在中断给药后可以恢复。研究 A8081007 中,8%的患者出现减少剂量相关的转氨酶升高,而研究 A8081001 和研究 A8081005 中这一比例为 3%。参与研究 A8081007、研究A8081001 和研究 A8081005 的患者中分别有 2 例(1%)、1 例(< 1%)和 5 例(< 1%)需永久停用本品治疗。 严重肝损害患者不应使用本品(见 【禁忌】 ) 。治疗的头 2 个月,每周执行一次肝功能检查(包括 ALT、AST 和总胆红素)监测,之后每月例行及在出现临床指征时执行一次,对于 2、3 或 4 级升高,则需要更加频繁地重复检查。 应根据 【用法用量】 和 【注意事项】 的建议对患者进行肝毒性监测和管理。 胃肠道影响 恶心、腹泻、呕吐和便秘是最常报告的胃肠道事件。恶心和呕吐的中位发生时间为 2 至 3 天。大多数事件都为轻度至中度,且在治疗 3 至 4 周后发生频率下降。支持性治疗应包括使用止吐药。腹泻和便秘的严重程度主要为轻度至中度。腹泻和便秘的支持性治疗应分别包括使用常用止泻药和通便药。 在使用克唑替尼的临床研究中有胃肠道穿孔事件的报告。在克唑替尼胶囊上市后使用过程中,有胃肠道穿孔致命性病例的报告(见 【注意事项】 )。 QT 间期延长 在研究 A8081007 和研究 A8081005 中,第 1 疗程第 1 天和第 2 疗程第 1 天 QTcF(按 Fridericia 法调整的 QT) 较基线值的平均变化分别为 8.3 ms 和 8.7 ms (QTcF 的双侧 90% CI 的上限分别为 13.1 ms 和 10.2ms,均小于 15 ms,因此 QTc 变化产生临床影响是不大可能的)。研究 A8081007 和 A8081005 中,分别有 5 例(3.4%)和 10 例(1.1%)患者记录到 QTcF500 ms,且这两项研究中 QTcF 较基线最高增加值60ms 的患者分别为 9 例(6.3%)和 38 例(4.3%)。 研究 A8081007 报告了 6 例(3.5%)出现全因果关系 3 级或 4级心电图 QT 间期延长的患者(见 【注意事项】 和 【药代动力学】 )。 QT 间期延长可导致心律失常,是导致猝死的一个风险因素。QT 间期延长的临床表现主要为心动过缓、眩晕和晕厥。电解质紊乱、脱水和心动过缓可进一步增加 QTc 间期延长的风险,因此,建议具有胃肠道毒性的患者定期监测 ECG 和电解质水平(见 【注意事项】 )。 心动过缓 研究 A8081007、研究 A8081001 和研究 A8081005 中,分别有 8 例(5%)、13 例(9%)和 108 例(10%)患者报告在治疗期出现全因果关系心动过缓。 研究 A8081007、A8081001 和 A8081005的 170、144 和 890 例患者中,分别有 19 (11%)、26 (18%)和90 (10%)例患者的心率<50 bpm。如要合并使用可引起心动过缓的药物,应进行仔细评估。出现症状性心动过缓的患者应按照“剂量调整”及“注意事项”章节中的建议进行管理(见 【用法用量】和 【注意事项】 )。 中性粒细胞减少症和白细胞减少症 研究 A8081007、研究 A8081001 和研究 A8081005 中,分别有 13%、6%和 11%接受克唑替尼治疗的患者出现 3 级或 4 级中性粒细胞减少症。 各级中性粒细胞减少症的中位发生时间分别为 43、 197 和 47 天,3 级或 4 级中性粒细胞减少症的中位发生时间分别为 165、 197 和 64 天。 研究 A8081007、 研究 A8081001和研究 A8081005 接受克唑替尼治疗的患者中,分别有 2%、1%和 3%因中性粒细胞减少症导致减少剂量。研究 A8081005中< 1%的患者因中性粒细胞减少症需永久停用本品治疗。研究 A8081001 和研究A8081007 中未出现因中性粒细胞减少症而永久停药的情况。克唑替尼的临床研究中出现发热性中性粒细胞减少症的患者少于 1%。 研究 A8081007 和研究 A8081005 中,各有 2%的患者出现 3 级或 4 级白细胞减少症;研究 A8081001 中这类患者的比例为< 1%。研究 A8081007、研究 A8081001 和研究 A8081005 中,各级白细胞减少症的中位发生时间分别为 64、75 和 43 天;3 级或 4 级白细胞减少症的中位发生时间分别为 373、299 和 75天。 研究 A8081007 和研究 A8081005 中,导致减少剂量的白细胞减少症的发生率为< 1%。研究 A8081001未出现因白细胞减少症而减少剂量的情况。研究 A8081007、研究 A8081001 和研究 A8081005 均无患 者因白细胞减少症而永久停药。 研究 A8081007 中,患者发生白细胞和中性粒细胞 3 级或 4 级减少的频率分别为 5%和 13%。研究A8081001 中,患者发生白细胞和中性粒细胞 3 级或 4 级减少的频率分别为< 3%和 8%。研究 A8081005 中,患者发生白细胞和中性粒细胞 3 级或 4 级减少的频率分别为< 3%和 8%。 应在每月和出现临床指征时监测包括白细胞分类计数的全血细胞计数,如果出现 3 级或 4 级异常或出现发热或感染, 应更加频繁地重复检查。 对于出现血液学实验室检查异常的患者, 请参见 【用法用量】 。 ** 需要特别说明的是,由于不同审评机构(FDA 以及 EMA)所选择统计数据的计算方式不同,因此美国说明书与欧盟说明书中的数据也显示有些许差异。
禁忌: 禁用于对克唑替尼或本品中任一成分 (见 【成分】 - 辅料名称 ) 过敏的患者。 禁用于严重肝损害患者 (见【注意事项】 )。
注意事项: ALK 阳性情况的评估 对患者是否为 ALK 阳性进行评估时,必须选择经充分验证且可靠的方法,避免出现假阴性或假阳性结果。 肝毒性 在三项主要临床试验中,接受克唑替尼胶囊治疗的 1225 例患者中有 2 例(0.2%)发生了药物引起的致命性肝毒性反应。7 例患者(0.6%)出现了 ALT 升高大于正常值上限 3 倍同时总胆红素升高大于正常值上限 2 倍而碱性磷酸酶正常。此外,109 例患者(9.2%)的 ALT 升高大于正常值上限五倍。8 例患者(0.7%)因转氨酶升高而需要永久停药。这些实验室结果通常没有症状,且一般在中断给药后可以恢复。转氨酶升高通常发生在治疗的前 2 个月内。 肝功能检查包括ALT、 AST和总胆红素,在治疗开始的最初两个月应每周检测一次,之后每月检测一次,并且根据临床状况对转氨酶水平升高的患者更频繁地进行重复检测转氨酶、碱性磷酸酶或总胆红素升高水平。根据表2的说明进行临时暂停给药、减量或永久停药。 (见【用法用量】和【不良反应】) 此外,欧盟说明书**还报告了下列注意事项: 随机研究 A8081007 中,克唑替尼治疗组中有 17%的患者观察到 3 级或 4 级 ALT 升高,而化疗组中这一比例为 4%。研究 A8081001 中有 7%的患者观察到 3 级或 4 级 ALT 升高,而研究 A8081005 中有 8%的患者观察到该情况。中断给药后,通常 3 级和 4 级升高均可恢复。随机研究 A8081007 中的 2 例患者(1%)、研究 A8081001 的 1 例患者(< 1%)以及研究 A8081005 的 5 例患者(< 1%)需永久性停止治疗。 间质性肺病(非感染性肺炎) 接受克唑替尼胶囊治疗的患者可能出现严重的、危及生命或致命性间质性肺病(ILD)/非感染性肺炎。在临床试验 A8081007, A8081001 和 A8081005 中(n=1225),31 例(2.5%)接受克唑替尼胶囊治疗的患者出现了不同级别的 ILD,11 例(0.9%)患者出现了 3 级或 4 级 ILD、6 例(0.5%)患者出现了致命事件。这些事件通常发生在开始治疗后的最初 2 个月内。 欧盟说明书**还指出:鉴别诊断间质性肺病样疾病时(如:非感染性肺炎、放射性肺炎、过敏性肺炎、间质性肺炎、肺纤维化、急性呼吸窘迫综合征[ARDS]、肺泡炎、肺浸润、肺炎、肺水肿、慢性阻塞性 肺病、胸腔积液、吸入性肺炎、支气管炎、闭塞性细支气管炎和支气管扩张)应考虑药物诱导的间质性肺病/肺炎。 应密切监测患者 ILD/非感染性肺炎的肺部症状指标。并排除其他潜在原因引起的 ILD/非感染性肺炎。一旦患者出现治疗相关的 ILD/非感染性肺炎,应永久停止克唑替尼的治疗 (参见【用法用量】及【不良反应】) QT 间期延长 接受克唑替尼胶囊治疗的患者可能出现 QTc 间期延长 (见【用法用量】和【药代动力学】) ,可导致室性心动过速(如:尖端扭转型室性心动过速)或猝死的风险增加。在临床试验中(n=1225),34 例(2.7%)患者出现 QTc 间期延长(所有级别),17 例(1.4%)患者在至少 2 个单独的 ECG 出现 QTc大于 500 ms。 先天性长 QT 综合征患者应避免服用克唑替尼胶囊。 对于充血性心力衰竭、 缓慢性心律失常和电解质异常患者, 以及正在服用抗心律失常药物或其它已知可致 QT 间期延长药物的患者, 使用本品治疗时应定期监测其心电图、 电解质和肾功能。 服用本品时, 应尽可能在第一次给药前密切监测 ECG 和电解质 (如:血钙、镁、钾),并建议定期监测 ECG 和电解质,尤其是在开始治疗时出现呕吐、腹泻、脱水或肾功能损害情况时。 QTc 大于 500 ms 或与基线相比的变化大于或等于 60 ms 并伴有尖端扭转型室速、多形性室性心动过速或严重心律失常症状/体征的患者应永久停用克唑替尼胶囊。必须立即咨询心内科医生的建议。在至少2 个单独的 ECG 上 QTc 大于 500 ms 的患者应暂停使用克唑替尼胶囊, 直到恢复至 QTc 小于或等于 480ms,然后继续按表 2 中描述的减少剂量 (参见【用法用量】和【药代动力学】) 。 心动过缓 欧盟说明书**中, 临床研究报告了 5%至 10%接受克唑替尼治疗的患者在治疗期间出现全因果关系心动过缓。 接受克唑替尼胶囊治疗的患者可能会出现有症状的心动过缓(如:晕厥、眩晕、低血压)。在不同的临床试验里接受克唑替尼治疗的 1174 例患者中,出现心动过缓且心率<50 次/分的比例为 11%。在研究A8081007 中, 2.9%接受 XALKORI 胶囊治疗的患者出现了 3 级晕厥, 接受化疗的患者未出现此类事件。欧盟说明书也报告了,直到开始治疗后数周,克唑替尼才对心率下降产生全面影响。 尽可能避免克唑替尼与其他已知可引起心动过缓的药物(如 β-受体阻滞剂、维拉帕米和地尔硫卓之类的非二氢吡啶类钙通道阻滞剂、可乐定和地高辛)同时使用。应定期监测心率和血压。如果出现不会 危及生命的症状性心动过缓,暂停使用克唑替尼胶囊直到恢复为无症状性心动过缓或心率为 60 bpm 或以上,重新评估合并用药,并调整克唑替尼胶囊的剂量。如果克唑替尼胶囊引起危及生命的心动过缓,应永久停用本药;如果与已知可引起心动过缓或低血压的合并用药有关,应暂停使用克唑替尼胶囊直到恢复为无症状性心动过缓或心率为 60 bpm 或以上,如果可以停用或调整合并用药的剂量,则可在频繁监测下继续使用克唑替尼胶囊 250 mg,每日一次 (见【用法用量】和【不良反应】) 。 胚胎毒性 根据克唑替尼胶囊的作用机制,妊娠妇女服用后可能会给胎儿带来伤害。在大鼠非临床研究中,在暴露量约等于人体临床推荐剂量(250 mg,每日两次)时克唑替尼胶囊具有胚胎毒性和胎儿毒性。目前 尚未针对妊娠妇女服用克唑替尼胶囊进行充分且良好对照的研究。若在妊娠期间服用克唑替尼胶囊,或患者在服药期间怀孕,则应告知其该药对胎儿的潜在危害 (见【孕妇及哺乳期妇女用药】 ) 。 ALK 检测 2013 年 6 月发布的《中国间变性淋巴瘤激酶(ALK)阳性非小细胞肺癌诊断专家共识》(2013 版)、《中国表皮生长因子受体基因突变和间变性淋巴瘤激酶融合基因阳性非小细胞肺癌诊断治疗指南》 (2013 版)推荐,目前针对 ALK 融合基因检测常用的方法主要有 3 种:荧光原位杂交(FISH)、基于聚合酶链反应(PCR)扩增基础上的技术和针对融合蛋白表达的免疫组织化学法(IHC)。应根据目 前 ALK 融合基因检测各种方法的优缺点、临床样本的特点和实验室的条件,按合理的检测流程,选择合适的检测方法。 在选择使用克唑替尼治疗的患者时,必须由受过培训的专业技术人员采用经充分验证过的检测方法诊断为 ALK 阳性非小细胞肺癌(NSCLC)。在临床研究 A8081005、A8081007 及 A8081014 中使用的是 雅培贸易(上海) 有限公司的 ALK 基因重组检测试剂盒(荧光原位杂交法)(Vysis ALK Break Apart FISHProbe Kit)。在中国,罗氏诊断产品(上海)有限公司的 Ventana anti-ALK 抗体诊断试剂盒(免疫组织化学法)、雅培贸易(上海)有限公司的 ALK 基因重组检测试剂盒(荧光原位杂交法)及厦门艾德生物医药科技有限公司的 EML4-ALK 融合基因检测试剂盒 (荧光 PCR 法) 均已经获得 CFDA 批准用于 ALK融合基因的检测。 此外,欧盟说明书**中还报告了以下注意事项: 中性粒细胞减少症和白细胞减少症 3 级或 4 级中性粒细胞减少症是克唑替尼临床研究 (研究 A8081007、 研究 A8081001 和研究 A8081005)报告的很常见的不良事件(6%-13%)。3 级或 4 级白细胞减少症是常见的不良事件(2%)(见【不良反应】) 。克唑替尼的临床研究中出现发热性中性粒细胞减少症的患者少于 1%。应在每月和出现临床指征时监测包括白细胞分类计数的全血细胞计数,如果出现 3 级或 4 级异常或出现发热或感染,应更加频繁地重复检查 (见【用法用量】)。 胃肠道穿孔 在使用克唑替尼的临床研究中有胃肠道穿孔事件的报告。在赛可瑞上市后使用过程中,有胃肠道穿孔致命性病例的报告 (见【不良反应】) 。 有胃肠道穿孔风险(憩室炎史、肿瘤转移至胃肠道、合并使用有确定的胃肠道穿孔风险的药物)的患者应慎用克唑替尼。 出现胃肠道穿孔的患者应停用克唑替尼。应告知患者胃肠道穿孔的最初体征,并建议患者在出现胃肠道穿孔时迅速就医。 视觉影响 参与研究 A8081007、研究 A8081001 和研究 A8081005 的患者出现视觉异常。如果视觉异常持续出现或加剧,应考虑进行眼科检查(如:视敏度、眼底检查和裂隙灯检查)(见【不良反应】)。 非腺癌成分的 NSCLC 有关具有非腺癌成分的 ALK 阳性 NSCLC 患者的资料有限。 ** 需要特别说明的是,由于不同审评机构(FDA 以及 EMA)所选择统计数据的计算方式不同,因此美国说明书与欧盟说明书中的数据也显示有些许差异。
孕妇及哺乳期妇女用药: 孕妇 基于克唑替尼胶囊的作用机制,妊娠妇女服用可能会给胎儿带来伤害。目前尚无对妊娠妇女服用克唑替尼胶囊进行足够的且良好对照的研究。在大鼠的非临床研究中,在暴露于近似于人体临床推荐剂量(250 mg,每日两次)的情况下具有胚胎毒性和胎儿毒性。对器官形成期间的妊娠大鼠和家兔给予克唑替尼,以研究药物对胚胎/胎儿发育的影响。当大鼠用药为50 mg/kg/天时(根据曲线下面积,大约 为推荐人体临床用药剂量的 0.6 倍),出现着床后流产增加。当大鼠用药剂量达 200 mg/kg/天(根据曲线下面积,大约为推荐人体临床剂量时的 2.7 倍)或家兔用药剂量达 60 mg/kg/天(曲线下面积约为推荐人体临床剂量时的 1.6 倍)时,胚胎的体重有所降低,但未出现致畸作用。 育龄妇女在服用克唑替尼胶囊进行治疗时应尽量避免怀孕。 服用本药的育龄妇女或服用本药的育龄妇女的伴侣,在治疗过程中以及完成治疗至少 90 天内应采取适当的方法进行避孕。若在妊娠期间服用本药,或患者或其伴侣在用药期间怀孕,则应告知其本品对胎儿具有潜在危害。 哺乳期妇女 目前尚不明确克唑替尼及其代谢物是否会从乳汁中分泌。由于多数药物通常都会从乳汁中分泌,以及婴儿若暴露于克唑替尼会发生潜在的严重不良反应,因此,决定哺乳期妇女是否终止哺乳或停止用药 非常重要。
儿童用药: 目前尚无儿科患者使用克唑替尼胶囊的有效性和安全性数据。 研究发现, 给予幼鼠克唑替尼 150 mg/kg/天,每日一次,连续 28 天后(根据曲线下面积,大约为 5.4 倍的推荐人体临床剂量) ,其长骨生长过程中骨形成减少。关于儿科患者的其他潜在毒性,尚未在幼年动物中进行评价。
老年用药: 研究A8081007中有27例 (16%) 接受克唑替尼胶囊治疗的患者年龄为65岁或65岁以上; 研究A8081005中有 152 例(16%)为 65 岁或 65 岁以上;研究 A8081001 中有 16 例(13%)为 65 岁或 65 岁以上。未见这些患者与年轻患者在安全性或有效性方面存在总体差异。
药物相互作用: 可能会增加克唑替尼血药浓度的药物 克唑替尼与 CYP3A 强抑制剂合用可能会导致克唑替尼血药浓度升高 (参见【药代动力学】) 。应避免合并使用下列 CYP3A 强抑制剂(包括但不仅限于):阿扎那韦、克拉霉素、印地那韦、伊曲康唑、酮康唑、奈法唑酮、奈非那韦、利托那韦、沙奎那韦、克拉霉素、泰利霉素、醋竹桃霉素和伏立康唑。而西柚或西柚汁也可能会增加克唑替尼的血药浓度,应避免同时食用。与中度 CYP3A 抑制剂合并用药 时应谨慎。 可能会降低克唑替尼血药浓度的药物 克唑替尼与 CYP3A 强诱导剂合用可能会导致克唑替尼血药浓度降低 (参见【药代动力学】) 。应避免合并使用下列 CYP3A 强诱导剂(包括但不仅限于):卡马西平、苯巴比妥、苯妥英钠、利福平、利福布丁和圣约翰草 。 克唑替尼可能改变其血药浓度的药物 克唑替尼在体内或体外均可抑制 CYP3A (参见【药代动力学】) 。服用克唑替尼的患者应避免与治疗指数较窄的 CYP3A 底物(包括但不限于阿芬太尼、环孢霉素、双氢麦角胺、麦角胺、芬太尼、匹莫齐特、奎尼丁、西罗莫司和他克莫司)合并使用。如果服用克唑替尼胶囊的患者需要合并使用这些治疗指数较窄的 CYP3A 底物,可能需要减少 CYP3A 底物的剂量,因为药物合用可产生不良反应。
药物过量: 目前尚无已知的克唑替尼胶囊药物过量的病例。目前尚无克唑替尼胶囊解毒剂。 药物相互作用 CYP3A 抑制剂 克唑替尼单剂量口服 150 mg,合并 CYP3A 强抑制剂酮康唑(200 mg,每日两次),克唑替尼的 AUC inf和 C max 值与单独服用克唑替尼相比,分别增加约 3.2 倍和 1.4 倍。但是目前尚未确立 CYP3A 抑制剂对稳态克唑替尼暴露量影响的大小 (参见【药物相互作用】)。 CYP3A 诱导剂 克唑替尼单剂量口服 250 mg,合并服用 CYP3A 强诱导剂利福平(600 mg,每日一次),克唑替尼的AUC inf 和 C max 与单独服用克唑替尼相比分别降低 82%和 69%。但是尚未确立 CYP3A 诱导剂对于稳态克唑替尼暴露量的影响的大小 (参见【药物相互作用】) 。 提高胃内 PH 值的药物 在正常受试者中,连续 5 日每日服用埃索美拉唑 40 mg 后,同时单剂量口服 250 mg 克唑替尼,未发现克唑替尼暴露量出现临床相关变化(AUCinf 降低 10%,Cmax 无变化)。 CYP3A 底物 合用咪达唑仑与克唑替尼(每日两次,每次 250 mg,连续服用 28 天)的患者的 AUC inf 与单独口服咪达唑仑时相比增加了 3.7 倍,这表明克唑替尼是 CYP3A 的一种中度抑制剂(参见【药物相互作用】)。 其他 CYP 底物 体外研究表明,尽管克唑替尼是 CYP1A2,CYP2C8,CYP2C9,CYP2C19 或 CYP2D6 等底物代谢的介导抑制剂,但在临床上不会发生药物相互作用。 克唑替尼是 CYP2B6 的体外抑制剂。因此,克唑替尼与主要经 CYP2B6 代谢的药物合并使用时可能会增加其血药浓度。 体外研究表明,尽管克唑替尼是 CYP1A2,CYP2B6,CYP2C8,CYP2C9,CYP2C19 或 CYP3A 底物代谢的介导诱导剂,但在临床上不会发生药物相互作用。 UGT 底物 体外研究表明,尽管克唑替尼介导抑制属于UGT1A1、UGT1A4、UGT1A6、UGT1A9或UGT2B7底物的药物代谢,但在临床上不会发生药物相互作用。 转运底物 在体外,临床相关浓度的克唑替尼会抑制 P-糖蛋白(P-gp) 。 因此,当克唑替尼与属于 P-糖蛋白底物的药物合并使用时可能增加其血药浓度。 体外研究表明,临床相关浓度的克唑替尼会抑制肝脏摄取转运蛋白、有机阳离子转运蛋白 1(OCT1)、肾脏摄取转运蛋白和有机阳离子转运蛋白 2(OCT2)。因此,当克唑替尼与属于 OCT1 或 OCT2 底物 的药物合并使用时可能增加其血药浓度。 体外研究发现, 临床相关浓度的克唑替尼不会抑制人类肝脏摄取转运蛋白 OATP1B1 或 OATP1B3 或者肾脏摄取转运蛋白 OAT1 或 OAT3。 对其他转运蛋白的作用 体外研究表明,临床相关浓度的克唑替尼不会抑制肝脏外排胆盐输出泵转运蛋白(BSEP)。 特殊人群 肝损害: 目前尚未对肝损害的患者使用克唑替尼的情况进行研究。由于克唑替尼主要在肝脏代谢,肝损害很可能升高克唑替尼的血浆浓度。 临床研究排除纳入 AST 或 ALT>2.5 倍的正常值上限或由于肿瘤肝转移而>5.0 倍正常值上限或总胆红素>1.5 倍的正常值上限的患者。因此,肝损害的患者使用克唑替尼胶囊进行治疗时应谨慎 。 对来自研究 A8081007、A8081005 和 A8081001 的数据进行群体药代动力学分析表明,基线总胆红素(0.1 至 2.1 mg/dL)或 AST 水平(7 至 124 U/L)不会对克唑替尼暴露量产生临床相关影响。 肾损害: 研究 A8081007、A8081005、A8081001 中轻度([CLcr]为 60 至 89 ml/分钟,N=433)和中度([CLcr]为 30 至 59 ml/分钟,N=137)肾损害患者的稳态谷浓度进行群体药代动力学分析,评估了克唑替尼的药代动力学。轻度或中度肾损害不会对克唑替尼暴露量产生临床相关影响。对 7 名无需透析的严重肾损害(CLcr<30 ml /分钟)患者及 8 名肾功能正常([CLcr] ≥ 90 ml/分钟)的患者进行了一项研究。所有患者都接受 250 mg 单次口服剂量的克唑替尼胶囊。相对于肾功能正常的患者,严重肾损害患者的克唑替尼平均 AUC inf 和平均 C max 分别升高 79%和 34%。 且观察到克唑替尼活性代谢产物的 AUCinf和 Cmax 也有类似变化 (见【用法用量】) 。 种族 :亚洲患者(N=523)和非亚洲患者(N=691)的克唑替尼暴露量不存在临床相关差异 。 年龄 :根据研究 A8081007、A8081005 和 A8081001 的群体药代动力学分析,年龄不会对克唑替尼的暴露量产生任何影响。 体重和性别 :根据研究 A8081007、A8081005 和 A8081001 的群体药代动力学分析,体重或性别不会对克唑替尼暴露量产生任何临床相关影响。 心脏电生理 研究对服用克唑替尼 250 mg,每日两次的所有患者的 QT 间期延长的可能性进行了评估。单剂给药后,达稳态时连续采集患者的三份心电图以评价克唑替尼对 QT 间期的影响。 通过对心电图自动记录的评估发现,1167 例患者中有 16 例(1.4%)QTcF≥500 ms(采用 Fridericia 法校正 QT) ,1136 例患者中有 51例(4.4%)其 QTcF 相比基线的增加≥60 ms。一项药动学/药效学分析表明 QTcF 增加具有浓度依赖性(见【注意事项】)。
贮藏: 30°C 以下保存。
有效期: 36个月 |