|
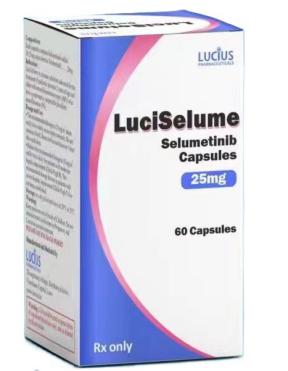
FDA批准司美替尼用于治疗1型神经纤维瘤病,伴有症状性、无法手术的丛状神经纤维瘤时间:2024-05-16 FDA(美国食品和药物管理局)在2020年4月10日批准了司美替尼(Selumetinib,商品名:KOSELUGO)用于治疗2岁及以上的患有1型神经纤维瘤病(NF1)且伴随有症状性、无法手术的丛状神经纤维瘤(PN)的儿科患者。这一决定基于SPRINT(NCT01362803)临床试验的积极结果,该试验由美国国家癌症研究所(NCI)资助,是一项开放标签、多中心、单臂试验,旨在评估司美替尼在治疗这类患者中的疗效和安全性。
司美替尼是一种激酶抑制剂,特别是针对MEK1和MEK2的抑制剂,这两种激酶在Ras-Raf-MEK-ERK信号通路中起到关键作用。该通路在多种癌症中被激活,包括NF1。通过抑制这一通路,司美替尼能够减少细胞增殖并促进细胞凋亡,从而在NF1患者的治疗中发挥作用。 SPRINT试验的结果显示,在接受司美替尼治疗的患者中,总体缓解率(ORR)达到66%,这意味着至少66%的患者的肿瘤体积在3-6个月内缩小了至少20%。所有接受治疗的患者均获得了部分缓解,且82%的缓解者持续缓解至少12个月。这一结果表明司美替尼在治疗NF1伴随PN的儿科患者中具有显著的疗效。 然而,司美替尼的使用也伴随着一些不良反应。在SPRINT试验中,最常见的不良反应包括呕吐、皮疹、腹痛、腹泻、恶心、皮肤干燥、疲劳、肌肉骨骼疼痛等。此外,司美替尼还可能引起心肌病、眼毒性(包括视网膜静脉阻塞、视网膜色素上皮脱离和视力受损)以及肌酐磷酸激酶升高等不良反应。因此,在使用司美替尼时,需要密切监测患者的不良反应情况,并根据需要调整剂量或停药。 总体而言,FDA对司美替尼的批准为患有1型神经纤维瘤病并伴随有症状性、无法手术的丛状神经纤维瘤的儿科患者提供了新的治疗选择。
司美替尼仿制药已在老挝上市,仿制药是一种治病的新选择,如需购买,可自行出国就医, “海得康”作为一个专业的医疗咨询平台,为患者提供有关该药物的详细信息和个性化建议。海得康有着丰富的国际新药动态知识和经验,能够为国内患者提供全球已上市药品的专业咨询服务。如有需要,可以拨打服务热线400-001-9769或海得康官方微信15600654560来获取帮助。请注意,所有关于药物的使用和副作用的信息都应仅作为参考,并不应替代医生的专业建议。在决定使用或更改任何药物治疗方案之前,务必与医生进行充分的沟通和讨论。
|