|
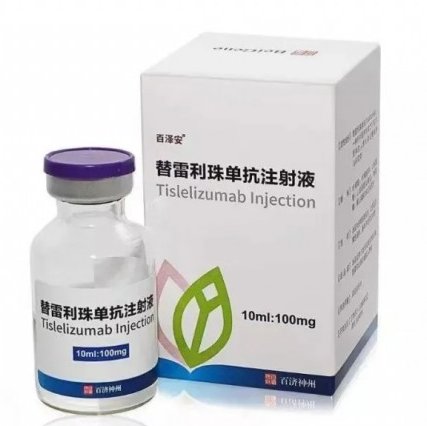
替雷利珠单抗治疗晚期/转移性食管鳞状细胞癌,国内医保报销条件时间:2024-03-19 在全球范围内,食管癌(EC)已成为癌症相关死亡的第六大常见原因,其中食管鳞状细胞癌(ESCC)作为最常见的组织学亚型,占比近90%。近日,美国食品和药物管理局(FDA)批准了一款名为替雷利珠单抗(Tevimbra,tislelizumab-jsgr)的创新药物,作为单一疗法,专门用于治疗经过不含PD-(L)1抑制剂的全身化疗后,仍患有不可切除或转移性ESCC的成年患者。预计Tevimbra将于2024年下半年在美国正式上市。
替雷利珠单抗是一种独特设计的人源化免疫球蛋白G4(IgG4)抗程序性细胞死亡蛋白1(PD-1)单克隆抗体。该药物对PD-1具有高亲和力和特异性结合能力,旨在最大限度地减少与巨噬细胞上Fc-gamma(Fcγ)受体的结合,从而有效协助身体的免疫细胞检测和对抗肿瘤。 FDA的此次批准是基于RATIONALE302试验的积极结果。该试验在意向治疗(ITT)人群中达到了主要终点,显示与化疗相比,Tevimbra在统计学和临床上均表现出显著的生存获益。在ITT人群中,接受Tevimbra治疗的患者中位总生存期(OS)为8.6个月,而化疗组仅为6.3个月。此外,Tevimbra还展现出优于化疗的安全性。 替雷利珠单抗的安全性数据表明,最常见的不良反应(≥20%)包括葡萄糖升高、血红蛋白降低、淋巴细胞减少等实验室异常,以及疲劳、肌肉骨骼疼痛、体重减轻等非实验室异常。值得注意的是,这些反应大多在可控范围内。 替雷利珠单抗的医保报销条件主要包括:患者必须患有至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤,或者是PD-L1高表达的含铂化疗失败(包括新辅助或辅助化疗12个月内进展)的局部晚期或转移性尿路上皮癌。只有满足这些特定适应症的患者,在使用替雷利珠单抗时才有可能享受医保报销。
海得康”发掘国际新药动态,为国内患者提供全球已上市药品的咨询服务,更多问题,请咨询海得康医学顾问,电话:400-001-9769,海得康官网微信:15600654560。
【友情提示:本文仅作为参考意见。用药期间随时与医生保持联系,随时沟通用药情况。图片侵权,请联系删除。】 |