新闻中心
|
|
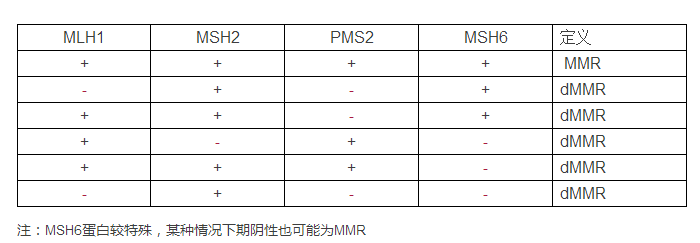
时间:2017-05-27 作者:pd1 FDA平地一声雷,朋友圈又被PD-1霸屏了——免疫药物PD1抑制剂Keytruda被批准用于“MSI-H/dMMR亚型”的实体瘤。 也就是说,很多癌种的病人不用再“眼红”黑色素瘤、非小细胞肺癌、头颈癌等等这些可以“名正言顺”从pd-1抑制剂上获益的肿瘤患者了,也不用再眼巴巴盼着FDA批准的适应症范围能大点再大点。 这一次,治疗的边界都被打破了,不管你的肿瘤来自何方,只要你符合某种基因突变类型,就能用! 精准医疗迈进了新时代,幸福来得太突然了,有木有? 但问题又来了。 这种MSI-H/dMMR亚型怎么测,哪里测?用药前是否还需要再测个PDL-1表达值?小尊可都帮你们打探好了。 这次获批基于一项纳入149名患者的临床试验,涵盖了15种癌症类型,结直肠癌(32位),子宫内膜癌(5位),胃癌(5位),胆管癌(3位),胰腺癌(5位),小肠癌(3位),乳腺癌(2位),前列腺癌(1位),食管癌(1位),小细胞肺癌(1位)。瘤种不同,却有一个共同点就是,肿瘤中都带有MSI-H或dMMR变异。 最后的效果也令人惊叹:39.6%的患者肿瘤明显缩小,其中部分缓解者有48人,完全缓解者有11人。出现缓解的患者中,持续缓解时间超过半年的比例超过了78%。要知道,PD-1抑制剂在之前那些已经获批的瘤种中,有效率也只有15%。 获批推荐剂量为:成人200mg/3周,儿童为2mg/kg,上限不超过200mg。 MSI-H意思是“微卫星不稳定性高”,dMMR的意思是“错配修复缺陷”。MMR是一种错配修复蛋白,其缺失则无法修复DNA复制过程中的错误,从而导致肿瘤细胞的基因组DNA中短串联重复序列发生改变,即微卫星不稳定性。 其实MSI-H/dMMR是pd-1抑制剂的一个有效生物标志物,在结直肠癌中最早得到过证实。NCCN指南2017版直肠及结肠版均推荐MSI-H/dMMR晚期/转移性结直肠癌患者可使用Keytruda作为二线治疗方案。 专业内容太艰涩,对于患者来说,最关心的就是怎么用。 毕竟MSI-H/dMMR亚型的肿瘤,在各种癌症中都是少数。比如晚期转移的结直肠癌中,只有5%左右是这种亚型。除此之外的另外之95%如果盲试PD1,结果可能只有一个——烧钱。 因此别看到结直肠癌、子宫内膜癌、胃癌……这些字样就脑子一热往前冲,而是要先搞懂自己是不是属于MSI-H/dMMR亚型。 目前国内有部分三甲医院开设了MSI/dMMR的检测,使用病理组织白片进行检测,检测时间约为1周左右。(据小尊了解,不少医院因为该检测的样本量低,成本高,一般也是外送至基因公司检测。各家医院及公司的技术上问题不大,都已经是很成熟的检测了。) 方法一:蛋白检测。可通过对肿瘤组织进行免疫组化检测,患者的化验单上结果会显示MLH1、MSH2、PMS2、MSH6四个蛋白的阴阳性,结果判定简单来说就是:除非四个蛋白皆为阳性(+),其他情况皆为dMMR。
方法二:DNA检测。通过多重荧光PCR+毛细管电泳检查肿瘤组织中的MSI,即检测微卫星不稳定性。MSI的报告结果通常为表明MSI-H(高不稳定性)/MSI-L(低不稳定性)或MSS(微卫星稳定)。 一般来说通过全血或肿瘤组织样本进行检测,目前有不少基因公司都有提供相关服务,检测周期大约5个工作日。 小尊预测,检测MSI-H/dMMR亚型之后恐怕会成为不少实体肿瘤患者诊断的“标配”。 注:是否需要测PDL-1表达值? 由于PD-1抑制剂药贵有效率又不高,因此国内患者大都会在用药前检测PDL-1的表达值,那么这类亚型患者是否仍需要做这类检测呢? |
|
|