|
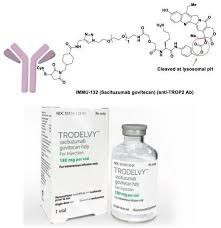
Gilead宣布戈沙妥珠单抗(Trodelvy)在转移性乳腺癌中的阳性新数据时间:2023-06-06 Gilead Sciences (Gilead)宣布了戈沙妥珠单抗(Trodelvy)的新数据,证明了HR+/HER2转移性乳腺癌患者Trop-2表达水平的临床疗效,这些患者在基于内分泌的治疗和至少两种化疗方面取得了进展。 Trop-2是一种在癌细胞表面发现的蛋白质,参与调节癌症生长和侵袭的几种细胞过程。它在大多数人类实体瘤中高度表达,包括超过90%的乳腺癌。 在3期TROPiCS-02研究的事后分析中,与医生选择的跨Trop-2表达水平的化疗相比,抗体-药物缀合物改善了无进展生存期、总生存期和客观缓解率。 TROPiCS-02中戈沙妥珠单抗的安全性与先前的研究一致,没有观察到新的安全性信号。这项事后分析表明,Trop-2在个体肿瘤中的表达水平不会影响戈沙妥珠单抗的疗效。 HR+/HER2-乳腺癌是最常见的乳腺癌类型,占所有新病例的70%左右,或每年全球近400,000例诊断。几乎三分之一的早期乳腺癌最终会转移,并且随着患者对基于内分泌的治疗产生耐药性,他们的主要治疗选择仅限于单剂化疗。
对基于内分泌的治疗产生耐药性的治疗前HR+/HER2转移性乳腺癌患者的预后很差,这些TROPiCS-02研究结果证明了戈沙妥珠单抗在Trop-2表达水平上的临床疗效。 目前,戈沙妥珠单抗已在40多个国家获得批准,用于治疗患有不可切除的局部晚期或转移性三阴性乳腺癌(TNBC)的成年患者,这些患者以前接受过两种或更多种全身治疗,其中至少一种用于转移性疾病。 美国食品药品监督管理局(FDA)也已同意优先审查戈沙妥珠单抗在患有不可切除的局部晚期或转移性HR+/HER2-乳腺癌的成年患者中的补充生物制剂许可申请,这些患者已经接受了基于内分泌的治疗和至少两种额外的系统性治疗。 2022年戈沙妥珠单抗获得中国国家药品监督管理局上市许可申请受理并被纳入优先审评品种,6月份在国内上市。由于在国内不久,所以患者在国内药房购买比较困难,具体请咨询当地医院药房。如果国内药房购买不到戈沙妥珠单抗可以通过国外渠道进行购买,国外的戈沙妥珠单抗只有原研药,没有仿制药,原研药有欧洲版、新加坡版和美版原研药,美版原研药价格高达36000左右,欧洲版和新加坡版原研药比美版便宜一半多,价格大约15000元左右,二者药物成分一致。 “海得康”发掘国际新药动态,为国内患者提供全球已上市药品的咨询服务,请咨询海得康医学顾问:400-001-9769,海得康官网微信:15600654560。
【友情提示:本文医药信息内容仅供参考,具体疾病治疗和用药请咨询医生评估,海得康不承担任何责任。本站图片来源于网络,侵权请联系删除。】 |