|
|
钟南山预判6月底或迎来今年第二波疫情高峰!辉瑞帕罗韦德/帕克洛维(Paxlovid)已退出医保目录,低价购买又如何“另辟蹊径”?时间:2023-05-26 钟南山:第二波疫情高峰可能六月底到来 5月22日,在2023大湾区科学论坛生物医药与健康分论坛上,共和国勋章获得者、中国工程院院士钟南山在谈及新冠疫情时表示,6月底或是今年第二波新冠疫情高峰。基于模型对全国2023年新冠第二波疫情(XBB)趋势预测显示,2023年5月底最高峰感染人数4000万/周,6月底达到约6500万/周。 钟南山介绍,无论有症状还是没有症状,如果体内新冠病毒对应的抗体增高,就说明人体曾被感染过。从这个角度看,根据测定,全国大概有85%的人感染过新冠病毒,约有11亿至12亿人。 根据相关实验室研究和新加坡等地的真实世界研究,新冠病毒感染后产生的抗体能在4-6个月的时间内起到保护人体的作用;但如果面对变异株XBB,其保护力可能会减弱,“从去年12月算起,实际看现在已经是到了这个时间了。”
辉瑞P药高价“出局” 2023年1月8日,2022年国家医保药品目录谈判工作正式结束,美国辉瑞高效新冠阻断药物帕罗韦德/帕克洛维(Paxlovid)因报价过高遗憾“出局”,这就意味着目前纳入临时医保的帕罗韦德/帕克洛维将在今年3月31日之后只能全额自费购买,无法享受报销优惠。 2021年12月,美国食品药品监督管理(FDA)局发布了辉瑞公司Paxlovid(nirmatrevir片剂和ritonavir片剂,共同包装用于口服)的紧急使用授权(EUA ),用于治疗成人和儿童患者(12岁及以上,体重至少40公斤或约88磅)的轻至中度冠状病毒疾病(新冠肺炎),这些患者的直接新型冠状病毒检测结果为阳性,并且具有发展为重度新冠肺炎的高风险,包括住院治疗或死亡。2022年2月,中国国家药品监督管理局紧急批准帕罗韦德/帕克洛维在国内上市,被纳入我国第九版、第十版新冠诊疗方案,用于治疗发病5天以内的轻、中型且伴有进展为重症高风险因素的成年患者。 根据美国FDA批准的EPIC-HR试验,帕罗韦德/帕克洛维以其高效阻止新冠病毒在体内引发重症的几率大大降低,由此帕罗韦德/帕克洛维在市面上作为抗新冠药物“独占鳌头”,但是其原研药价格很高,加上药品无法满足患者供求,曾一盒价格被“黄牛”炒作到5万元的天价,对于普通患者来说根本无法承受,那需要或者想要给家里老人或有基础疾病患者储备帕罗韦德/帕克洛维又怎么“另辟蹊径”来获取呢?
多版本仿制药解决患者诉求 随着辉瑞原研药Paxlovid的问世,多个版本的仿制药也如雨后春笋般相继出现,虽然不是辉瑞原厂生产的,但是这些仿制药基本上都是由美国辉瑞公司授权或者当地政府批准上市的,价格方面比原研药要低很多。 1.孟加拉Bexovid(美国辉瑞官方授权) 孟加拉Beximco Pharmaceuticals Limited宣布推出辉瑞新冠肺炎治疗药物Paxlovid的全球首个仿制药版本(Nirmatrelvir和Ritonavir片剂,共同包装用于口服),该药物于2021年12月22日获得美国FDA的紧急使用授权(EUA)。孟加拉国药品管理总局(DGDA)已批准紧急使用口服抗病毒药物治疗成人和12岁及以上儿童的轻中度新冠肺炎。这种新型抗病毒药丸在防止高危患者住院和死亡方面显示出近90%的有效性,辉瑞最近的数据表明,该药物在对抗快速传播的冠状病毒变异体方面保持了其有效性。Beximco Pharma将首先在孟加拉国以Bexovid品牌销售该产品。
2.孟加拉Paxovir&孟加拉Jupitavir(孟加拉药监局DGDA批准上市) 孟加拉Eskayef Pharmaceuticals Ltd于2022年在孟加拉本地市场推出全球首个辉瑞Paxlovid的仿制药Paxovir。Paxovir可用于年龄在12岁及以上、出现轻度至中度症状的已接种和未接种新冠肺炎患者。 孟加拉Incepta Pharmaceuticals Limited将以品牌名Jupitavir销售辉瑞帕罗韦德/帕克洛维仿制药物。药品管理总局(DGDA)批准了该药物的紧急使用授权,用于治疗轻中度新冠肺炎患者,包括成人和12岁及以上的儿童。
3.印度Paxzen(印度药监局CDSCO批准上市) 印度Zenara Pharma公司宣布推出了Nirmatrelvir和Ritonavir片剂,作为轻度至中度新冠肺炎症状患者的治疗选择。Zenara Pharma已获得印度中央药品标准控制组织(CDSCO)的批准,可以生产和销售该产品。这款药物将以“Paxzen”的品牌名称出售,由Zenara在海德拉巴的美国食品药品管理局和欧盟批准的最先进工厂生产。
4.印度Paxista (蓝盒) 印度版Paxista(蓝盒)由印度仿制药厂Azista制药生产,其活性成分Nirmatrelvir 150MG和Ritonavir 100 MG被批准用于紧急情况。该药物适用于治疗新型冠状病毒病毒检测呈阳性的成人和儿科患者(年龄> 12岁,体重> 40公斤)的轻至中度冠状病毒疾病,这些患者具有较高的进展风险,包括住院或死亡。
帕罗韦德/帕克洛维高效“阻击”新冠病毒进入人体发展为重症 根据美国FDA批准的基于支持EUA的临床试验证明了5天疗程的帕罗韦德/帕克洛维的益处。这项研究表明,在具有进展为严重疾病的高风险的非住院患者中,使用帕罗韦德/帕克洛维治疗将住院或死亡的风险降低了88%。其他已批准的(Veklury [remdesivir])或已授权的(Lagevrio [molnupiravir])抗病毒药物的临床试验也证明了住院和死亡的减少。 帕罗韦德/帕克洛维被批准用于治疗成人和儿童患者(12岁及以上,体重至少40公斤或约88磅)的轻至中度新冠肺炎,这些患者的新型冠状病毒病毒直接检测结果为阳性,他们具有发展为重度新冠肺炎的高风险,包括住院治疗或死亡。
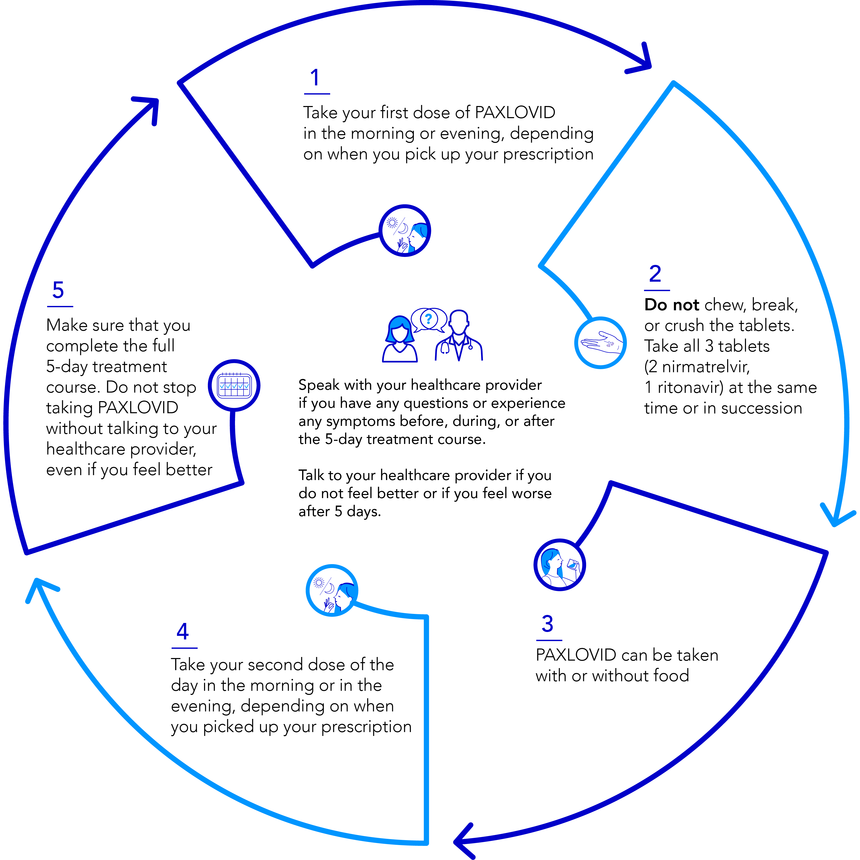
帕罗韦德/帕克洛维用药说明及注意事项 1.用药方法: 帕罗韦德/帕克洛维是奈玛特维(Nirmatrelvir)与利托那韦(Ritonavir)片剂包装在一起的片剂,奈玛特维必须与利托那韦联合用药。使用方法主要有以下几点: •在诊断出新冠肺炎病后并在症状出现后5天内尽快开始帕罗韦德/帕克洛维治疗。 •与食物一起或单独口服。 •剂量:300mg奈玛特维(两片150 mg片剂)与100 mg利托那韦(一片100 mg片剂),三片片剂一起服用,每天两次(12小时一次),持续5天。 •中度肾功能损害(eGFR ≥30至< 60mL/min):150 mg 奈玛特维(一片150mg片剂)与100 mg利托那韦(一片100 mg片剂),两种片剂一起服用,每天两次(12小时一次),持续5天。 •严重肾功能损害(eGFR <30 mL/min)患者不建议使用帕罗韦德/帕克洛维。 •严重肝功能损害(Child-Pugh C类)的患者不建议使用帕罗韦德/帕克洛维。 2.不良反应: 不良事件(发生率≥1%且受试者差异≥5)为发育异常、腹泻、高血压和肌痛。 3.禁忌症: •对活性成分(奈玛特维或利托那韦)或任何其他成分有临床意义的超敏反应病史。 •与高度依赖CYP3A进行清除的药物联合给药,对于这些药物,浓度升高与严重和/或危及生命的反应有关。 •与强效CYP3A诱导剂联合给药时,奈玛特维或利托那韦血浆浓度显著降低可能与病毒学应答丧失和可能的耐药性相关。 4.注意事项: •帕罗韦德/帕克洛维与某些其他药物合用可能导致潜在的显著药物相互作用。 •超敏反应:帕罗韦德/帕克洛维曾出现过过敏反应和其他超敏反应。如果出现具有临床意义的超敏反应或过敏反应的体征和症状,立即停用帕罗韦德/帕克洛维,并开始适当的药物治疗和/或支持性护理。 •肝毒性:接受利托那韦治疗的患者出现肝转氨酶升高、临床肝炎和黄疸。 •HIV-1耐药性:在HIV-1感染未控制或未确诊的个体中,使用帕罗韦德/帕克洛维可能导致HIV-1产生HIV蛋白酶抑制剂耐药性的风险。
帕罗韦德/帕克洛维上市及价格情况 辉瑞帕罗韦德/帕克洛维原研药已经在国内上市,由于纳入的临时医保目录已经于2023年3月31日过期,所以无法进行医保报销,患者可以到医院药房进行购买,条件是必须是感染阳性患者并且凭借医生开具的处方,价格大约在2500元左右,具体价格及报销比例可以咨询当地药房或者医保局,但是由于药物紧缺所以购买是比较困难的。 国外的帕罗韦德/帕克洛维仿制药有多个版本,不失为一个好的选择:孟加拉辉瑞官方授权的仿制药Bexovid价格在1500元左右;孟加拉当地政府授权的仿制药Paxovir和Jupitavir大约在1500元左右;印度当地政府授权的仿制药Paxzen价格在1000元左右,以及印度版仿制药Paxista (蓝盒)价格在800元左右。原研药与仿制药的药物成分基本一致。 参考资料:1.FACT SHEET FOR HEALTHCARE PROVIDERS:EMERGENCY USE AUTHORIZATION FOR PAXLOVIDTM. 2.Coronavirus (COVID-19) Update: FDA Authorizes First Oral Antiviral for Treatment of COVID-19. 3.Eskayef launches first US FDA-approved oral Covid medicine in Bangladesh. 4.Paxovir (nimatvir/ritonavir) is listed in Bangladesh to treat Covid-19 infection. 5.Beximco Pharma introduces generic version of Pfizer’s Paxlovid; the first US FDA approved oral therapy for Covid-19 treatment. 6.Zenara Pharma launches Paxzen tablet against mild to moderate COVID. “海得康”发掘国际新药动态,为国内患者提供全球已上市药品的咨询服务,请咨询海得康医学顾问:400-001-9769,海得康官网微信:15600654560。
【友情提示:本文医药信息内容仅供参考,具体疾病治疗和用药请咨询医生评估,海得康不承担任何责任。本站图片来源于网络,侵权请联系删除。】 |