|
Paxlovid是否已获得FDA批准?时间:2024-05-31 · 是的,Paxlovid确实获得了FDA的批准。 · Paxlovid在2023年5月25日获得了FDA的批准,专门用于治疗存在高风险进展为严重COVID-19(包括住院或死亡)的轻至中度COVID-19成年患者。 · 根据紧急使用授权(EUA),Paxlovid还被允许用于治疗12至18岁且存在进展为重症COVID-19高风险的轻度至中度患者。 · 然而,Paxlovid并未被批准用作COVID-19的暴露前或暴露后预防药物。
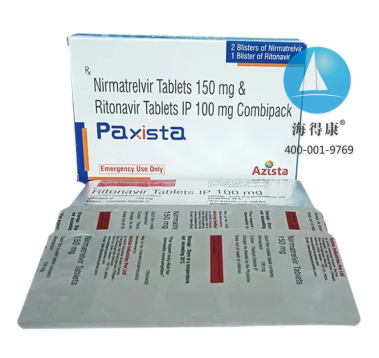
Paxlovid是如何发挥作用的? · Paxlovid是一个组合包装,其中包含nirmatrelvir片剂和利托那韦片剂。在SARS-CoV-2病毒检测呈阳性后,一旦出现COVID-19疾病的初期症状,就应立即口服这些药物。 · Nirmatrelvir的主要作用是阻断冠状病毒复制所必需的酶(即SARS-CoV-2-3CL蛋白酶)。 · 通过阻止病毒自我复制,可以减轻症状的严重程度,进而降低高危患者的住院和死亡风险。 · 利托那韦,原本是一种用于治疗艾滋病毒的药物,在这里它被用来减缓nirmatrelvir的代谢速度,帮助nirmatrelvir在体内保持更长时间的高浓度,从而增强其疗效。 Paxlovid对COVID-19的治疗效果如何? · 对于处于COVID-19进展为严重疾病高风险的成年患者,如果在出现COVID-19症状的前3天内开始使用Paxlovid,它可以将因COVID-19住院或死亡的风险降低86%。这一结论来源于EPIC-HR研究(NCT04960202),这是一项2/3期、随机、双盲、安慰剂对照试验,受试者为实验室确诊为SARS-CoV-2感染且有症状的非住院成人患者。 · Paxlovid由两种共同包装的药物组成:nirmatrelvir(以前称为PF-07321332)和利托那韦。 · Paxlovid为口服药物,建议在出现COVID-19症状的初期就立即服用。 · Paxlovid旨在帮助减少症状的数量和严重程度,或者避免可能导致住院或死亡的严重疾病发生。
据悉,帕克洛维的仿制药已在印度正式上市。对于需要购买此药的患者来说,现在有了更多的选择。若考虑购买此药,患者可以选择前往国外就医,并在当地合法购买该药品。仿制药为那些寻求更经济、有效治疗方案的患者带来了希望。“海得康”作为一个专业的医疗咨询平台,有着丰富的国际新药动态知识和经验,能够为国内患者提供全球已上市药品的专业咨询服务。如有需要,可以拨打服务热线400-001-9769或海得康官方微信15600654560来获取帮助。 请注意,所有关于药物的使用和副作用的信息都应仅作为参考,具体用药还请务必与医生进行充分的沟通和讨论。
|